1.Основные формулы термодинамики
1).Условные обозначения
| Обозначение | Название величины | Размерность / Значение | Формула |
|---|---|---|---|
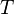 | Абсолютная температура | K | |
 | Давление | Па | |
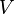 | Объём | м³ | |
 | Средняя энергия молекулы | Дж | |
 | Средняя кинетическая энергия молекулы | Дж | |
 | Масса | кг | |
 | Молярная масса | кг/моль | |
 | Постоянная Авогадро | 6.0221415(10)·1023 моль-1 | |
 | Постоянная Больцмана | 1.3806505(24)·10−23 Дж/К | |
 | Газовая постоянная | 8.314472(15) Дж/(К·моль) |  |
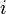 | Число степеней свободы молекулы | - | |
 | Количество вещества в  -й компоненте -й компоненте  -компонентной смеси -компонентной смеси | моль | |
 | вектор с координатами  | моль | |
 | Химический потенциал  -й компоненты -й компоненты  -компонентной смеси -компонентной смеси | Дж/моль | |
 | Внутренняя энергия | Дж | |
 | Энтропия | Дж/К | |
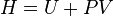 | Энтальпия | Дж | |
  | Изохорно-изотермический потенциал (свободная энергия Гельмгольца) | Дж | |
 | Изобарно-изотермический потенциал (свободная энергия Гиббса, свободная энтальпия) | Дж | |
 | Работа, совершённая газом | Дж | |
 | Тепло, переданное газу | Дж | |
 | Молярная теплоёмкость газа при постоянном давлении | Дж/(К·моль) | |
 | Молярная теплоёмкость газа при постоянном объёме | Дж/(К·моль) | |
 | Удельная теплоёмкость | Дж/(К·кг) | |
 | Показатель адиабаты | - |  |
2).Формулы термодинамики идеального газа
| Уравнение состояния идеального газа (уравнение Клапейрона—Менделеева) |  |
| Изменение внутренней энергии газа | 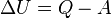 |
| Работа газа |  |
| Средняя энергия молекулы газа |  |
| Средняя кинетическая энергия молекулы газа: |  |
| Внутренняя энергия газа |   |
| Теплоёмкость газа при постоянном объёме |  |
| Теплоёмкость газа при постоянном давлении |  |
Информация взята с сайта ru.wikipedia.org